 |
 |
臨床家の行動変革の指針として開発されたEvidence-based medicine (EBM)だが,現在では臨床医学実践の世界標準となっている1,2).
EBMの創始者SackettらはEBMの行動目標を5つのステップに分けた2,3).すなわち,
1)問題点の抽出
2)情報(文献)の収集
3)批判的吟味critical appraisal
4)結果の患者への適用
5)以上のステップの評価
である.
多忙な日常診療において,個人の医師が2, 3)のステップを行うことは大変な労力を要するため,一般的にはレビュー・グループにより行われる.この作業及び結果をシステマティック・レビュー(systematic
review, 以下SR)という4).予め基準を設定した上で情報収集と批判的吟味を効率的に行い,最終的に一定の結論をもって要約する.SRにより「現在までに何が分かっており,何が分かっていないか,現在・未来において何をなすべきか」が明確になる.
皮膚科学における最大のEBM推進者,英国Nottingham大学のWilliamsらは英国医師会雑誌編集部のEBM 2次資料"Clinical Evidence"に協力し,アトピー性皮膚炎に関するSRを発表している5).また彼らは英国国民保健サービス(National Health Service, NHS)の医療技術評価プログラムの一環として予備的SRを公表している6).
WilliamsらのSRも現時点では中間報告的な未完成なものであり,各研究のエビデンスとしての質のレベル評価は行われていない.また言語的な問題から本邦の情報がほとんど収集されていない.今回,我々はさらに新しい文献を徹底的に検索・収集し,質を評価し,本邦の実情に合わせたSR作成を行った. |
 |
 |
 |
SR作成過程は国際的なEBM支援組織コクラン共同計画により標準化されている(表1)7).また,完成したSRはQUOROM(Quality of Reporting of Meta-analysis)声明により示された標準により評価される(表2)8).今回のSR作成過程,即ち,対象論文の基準,検索方法,研究の質の評価,解析の要約においては,これらの国際標準を可及的に満たすよう配慮した.
A. 対象論文の基準
ランダム化比較試験(randomized controlled trial, 以下RCT),対照のある非RCT試験(比較臨床試験,clinical controlled
trial, 以下CCT),コホート試験,症例対照試験(case control study),症例集積研究を可及的に収集することとした.
B. 情報 (文献)の検索と収集
PubMed,医学中央雑誌などのデータベースから電子サーチを行った.検索方法,検索式はできるだけ詳細に記載することとした.さらに,関連雑誌を可及的に手作業検索した.
C. エビデンスの質の評価
エビデンスの質の評価に関してはいくつかの分類表が考案されて来た(表3)(表4)(表5)2).これらは簡明であるが,治療,予後,検査等の領域に応じて研究デザインが異なるにも関らず,一律に評価しているという問題点がある.そこで,現在発表されている分類表として最も詳細かつ厳密なOxford大学EBMセンター分類を参考にすることとした(表6)9).しかし,複雑に過ぎるため,何度もの検討を加え,その要約版を考案した(表7).
エビデンスの質分類には,いまだ専門家の間でも論議がある.Williamsらも,そのシステマティック・レビュー5,6)においてエビデンスの質のレベルを評価することを躊躇しているが,我々はあえて今回のレビュー事業においてエビデンスの質評価を行うこととした.ただし,これは現時点での,あくまでも暫定的な評価であり,今後の世界動向により評価が変化することもあり得る.
D. 評価フォームの作成
基本的にはWilliamsらのSR5,6)の表を参考にしたが,上述のコクラン共同計画のSR作成過程表(表1)7),QUOROM声明のチェックリスト(表2)8),さらにRCT論文評価の国際標準となっているCONSORT
(Consolidated Standards of Reporting Trials)声明(表8)10)の各項目を可及的に満足する評価フォームを作成した(表9).
E. 批判的吟味
前記評価フォームに則って,各文献を評価し,一定の結論を出した.Williamsらにより指摘されている以下の問題について,特に検討した5,6).
1)RCT自体が少ない
2)脱落例が多い
3)現代臨床疫学では常識となっている,割り付けのままの(脱落例込みの)解析(治療企図解析,intention to treat analysis, ITT)が行われているものが少ない
4)盲検化(マスク化),ランダム化したと記載されていても,その方法が示されていない
5)データの実数や信頼区間が示されていないものが多く統計学的評価が困難
6)アウトカム評価項目が一定しておらず結論の導出が困難
F. 左右比較試験(left-right comparison)の問題
皮膚科領域には同一個体内比較(intra-individual comparison)あるいは左右比較を行った論文が多い.これらのエビデンスの問題点に対し,しばしば批判が投げかけられて来た.Williams教授との対談により,今回はこれらの試験も通常のRCT,あるいは対照試験と同様に扱うこととした(付録参照). |
 |
▼表1. コクラン共同計画におけるシステマティック・レビュー作成過程(文献7より)

▼表2. QUOROM声明のシステマティック・レビュー・チェックリスト(要約)(文献8より)

▼表3. 米国予防医療サービス特別研究班の分類(1991)

▼表4. 米国保健政策研究局(旧AHCPR,現AHRQ)の分類(1993)

▼表5. Gray(Oxford大)の分類(1997)

▼表6. Oxford大学EBMセンターの分類(文献9より)
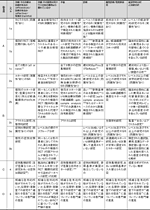
▼表7. Oxford大学EBMセンター分類の要約版(RCT: randomized controlled trial, ランダム化比較試験, SR: systematic review)

▼表8. CONSORT声明のRCT論文チェックリスト(要約)(文献10より)

▼表9.

|
 |
今回、本邦皮膚科において初めてシステマティック・レビューが作成されたことには大きな意義があると考える.種々の問題点が残っていることを承知の上でエビデンスの質のレベル評価を行っていることを理解して頂きたい.今後,これらは新しい論文の追加に伴い更新されて行くであろう.
臨床疫学的にRCTが最も妥当性が高いのだが,RCTが行い難い臨床分野があるのも当然であり,そのような場合,次善のエビデンスから順次適用して行くべきである.
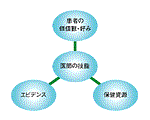
EBMでは,エビデンス(要素1)だけでなく,医師としての技能(要素2),患者の価値観・好み(要素3),保健資源(要素4)といった要素を統合することが目指されている(図1).この点をよく理解した上で,評価フォームに記載された治療を適正に運用して頂きたい.
|
 |
▼図1.
 |
 |
SRは定期的な更新が必要である.今後,既存の診療ガイドラインを補完するものとして,さらにグローバルスタンダードを満たすSRに発展させていく必要がある.今後の課題としては以下の点が挙げられる.
A. メタアナリシス meta-analysis
SRにおいて複数の研究結果の代表値を統計学的に統合すること(これを「定量的メタアナリシス」,SRを「定性的メタアナリシス」と呼ぶこともある).代表的手法にPeto法,Mantel-Haenszel法,DerSimonian-Laird法等がある11,12).
B. 決断分析decision analysisと費用効果分析cost-effectiveness analysis
メタアナリシスによりデータを統合して診療方針を決定するための統計学的手法を決断分析という.決断分析において決断樹を作成し,予測される転帰が達成できる費用を指標とする費用効果分析が行われる.メタアナリシス,決断分析,費用効果分析により医療情報が最終的に統合される11).
|
 |
 |
 |
1) Gray JAM: Evidence-Based Healthcare, Churchill Livingstone, a division of Harcourt Brace and Company Ltd, London, 1997 (邦訳. 久繁哲徳監訳: 根拠に基づく保健医療, じほう, 東京, 2000)
2) 厚生省健康政策局研究開発振興課医療技術情報推進室監修: わかりやすいEBM講座, 厚生科学研究所, 東京, 2000
3) Sackett DL, Richardson WS, Rosenberg W, Haynes RB: Evidence-based Medicine: How to Practice and Teach EBM, 2nd ed., Churchill Livingstone, a division of Harcourt Brace and Company Ltd, London, 2000 (邦訳. Evidence-based Medicine-EBMの実践と教育, エルゼビア・サイエンス, 東京, 2003)
4) 別府宏圀, 津谷喜一郎編: コクラン共同計画資料集, 第2版, サイエンティスト社, 東京, 1998
5) Smethurst D, Macfarlane S: Atopic Eczema, In Clinical Evidence, Issue 9, BMJ
Publishing, London, 2002 (邦訳. Clinical Evidence翻訳委員会訳:クリニカル・エビデンス, 日経BP, 東京, 2004, p1972-1990)
6) Hoare C, Li Wan Po A, Williams H: Systematic Review of Treatments for Atopic Dermatitis, Health Technology Assessment, 4(37), 2000
7) Clarke M, Oxman AD (eds): Cochrane Reviewer’s Handbook 4.1.5, In The Cochrane Library, Issue 2, Update Software, Oxford, 2002
8) Moher D, Cook DJ, Eastwood S: Improving the quality of reports of meta-analysis of randomized controlled trials: the QUOROM statement, Lancet, 354:1896-1900, 1999
9) Phillips B, Ball C, Sackett D, Haynes B, Straus S, McAlister F: Level of Evidence, March 2002, Evidence-based On-call homepage (http://www.eboncall. co.uk/), 2002
10) Moher D, Schultz KF, Altman DG: The CONSORT statement: revised recommendations for improving the quality of reports of parallel-group randomized trials, Lancet, 357: 1191-1194, 2001
11) Petitti DB:Meta-Analysis, Decision Analysis, and Cost-Effectiveness Analysis: Methods for Quantative Synthesis in Medicine, Oxford University Press, Oxford, 1994 (邦訳:福井次矢, 青木則明訳: EBMのためのデータ統合型研究―メタ分析, 決断分析, 費用効果分析の理論と実際. メディカル・サイエンス・インターナショナル, 東京, 1999)
12) 丹後俊郎:メタアナリシス入門:エビデンスの統合をめざす統計手法, 医学統計学シリーズ第4巻, 朝倉書店, 東京, 2002 |
 |
 |
|
|